New Lung Cancer Treatments 2022
Last updated: 18 March 2025
You can legally access new medicines, even if they are not approved in your country.
Learn howWhat is Lung Cancer?
Lung cancer begins in the lungs and may spread to lymph nodes or other organs in the body. Lung cancers usually are grouped into two main types:small cell and non-small cell. These types of lung cancer grow differently and are treated differently. Non-small cell lung cancer is more common than small cell lung cancer. Cancer from other organs also may spread to the lungs. When cancer cells spread from one organ to another, they are called metastases. 1
Can Lung Cancer be cured?
Treatment for lung cancer depends on several factors such as the type of cancer, where the tumors are located, the stage of cancer, and the patient’s overall health. There is always a chance that lung cancer can recur even after it has been in remission for years or decades.2
How is Lung Cancer treated?
The treatment choice for lung cancer depends on the type of lung cancer and how far it has spread. People with non-small cell lung cancer can be treated with surgery, chemotherapy, radiation therapy, targeted therapy, or a combination of these treatments. People with small cell lung cancer are usually treated with radiation therapy and chemotherapy.
- Surgery. An operation where doctors cut out cancer tissue.
- Chemotherapy. Using special medicines to shrink or kill the cancer.
- Radiation therapy. Using high-energy rays (similar to X-rays) to kill the cancer.
- Targeted therapy. Using drugs to block the growth and spread of cancer cells.
What are the newest Lung Cancer Treatments?
There are several approved Lung Cancer treatments options. Here are some of them:
Gavreto (pralsetinib)4
Gavreto (pralsetinib) is a kinase inhibitor (chemotherapy) indicated for the treatment of adult patients with RET fusion-positive non-small cell lung cancer (NSCLC) that has spread (metastasized).
Gavreto (pralsetinib) was approved by The Food and Drug Administration (FDA), USA, for the treatment of patients with metastatic RET fusion-positive NSCLC on September 4, 2020.
The FDA granted Breakthrough Therapy designation to Gavreto for the treatment of advanced RET fusion-positive NSCLC.
Retevmo (selpercatinib)5
Retevmo (selpercatinib) is a kinase inhibitor (chemotherapy) indicated for the treatment of RET fusion-positive non-small cell lung cancer (NSCLC) that has spread (metastasized) in adults.
Retevmo (selpercatinib) was approved for the treatment of lung and thyroid cancers with a genetic mutation or fusion in the RET gene by The Food and Drug Administration (FDA), USA, on May 8, 2020.
The FDA approval was given under Accelerated Approval. The FDA also granted Retevmo Priority Review and Breakthrough Therapy designation, to promote development of drugs that fulfill an unmet medical need Additionally, Retevmo received Orphan Drug designation, which is intended to encourage the development of drugs for the treatment of rare diseases.
Tabrecta (capmatinib)6
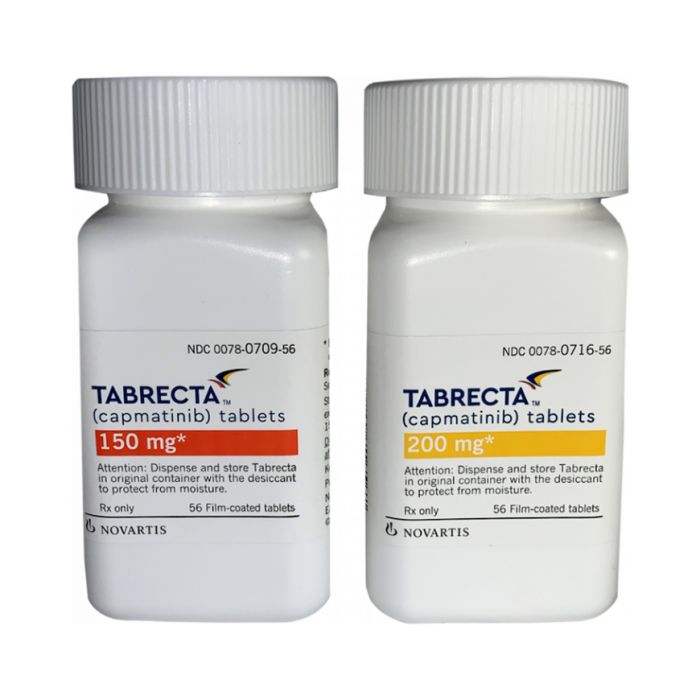
Tabrecta (capmatinib) is a medication used for the treatment of adults with metastatic non-small cell lung cancer (NSCLC) whose tumors have a mutation that leads to mesenchymal-epithelial transition exon 14 (METex14) skipping as detected by an FDA-approved test. It is available in tablet form each containing 150 mg or 200 mg capmatinib.
Tabrecta (capmatinib) was approved for the treatment of adult patients with metastatic non-small cell lung cancer (NSCLC) whose tumors have a mutation that leads to mesenchymal-epithelial transition METex14 skipping by the Food and Drug Administration (FDA), USA on May 6, 2020 and by the Pharmaceutical and Medical Devices Agency (PMDA), Japan on June 29, 2020.
The FDA granted accelerated approval and granted Priority Review, Breakthrough Therapy and Orphan Drug designation to Tabrecta (capmatinib), which is intended for the safe and effective treatment of rare diseases, and for drugs that have benefits over current treatment options.
Zepzelca (lurbinectedin)7
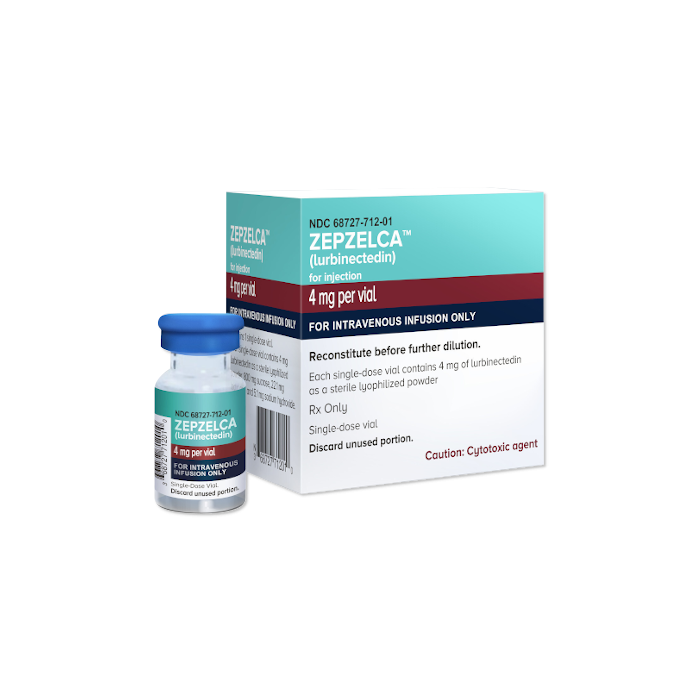
Zepzelca (lurbinectedin) is a type of chemotherapy indicated to treat adult patients with small cell lung cancer (SCLC) that is metastatic, i.e. cancer that has spread to other parts of the body, and that does not respond (anymore) to treatment with chemotherapy that contains platinum.
Zepzelca (lurbinectedin) was approved by The Food and Drug Administration (FDA), USA on June 15, 2020 with an accelerated approval for the treatment of adult patients with metastatic small cell lung cancer that progressed on or after platinum-based chemotherapy.
Tepmetko (tepotinib)8
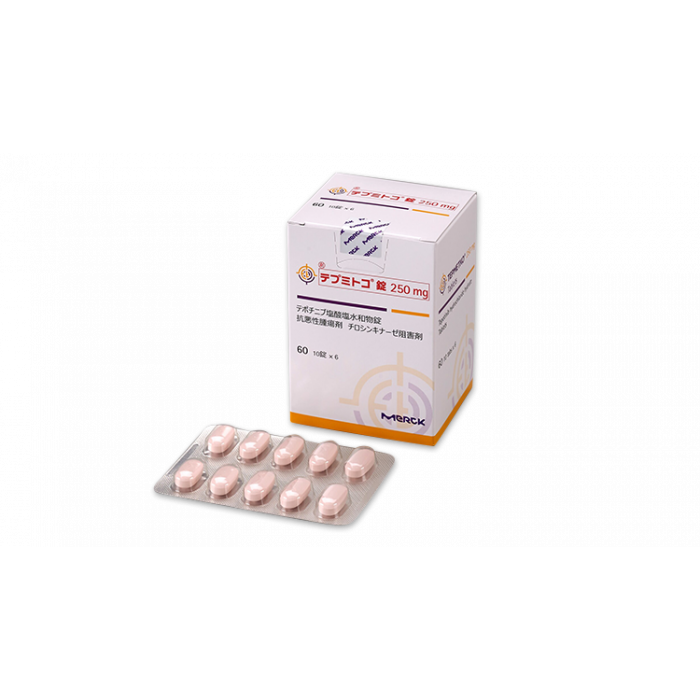
Tepmetko (tepotinib) is a MET inhibitor indicated for the treatment of advanced or recurrent non-small cell lung cancer (NSCLC) in adults with MET exon 14 (METex14) skipping mutations. This is the first regulatory approval globally for an oral MET inhibitor indicated for the treatment of advanced NSCLC harboring MET gene alterations.
Tepmetko (tepotinib) was approved in Japan by the PMDA on the 25th of March 2020, for line-agnostic treatment of advanced non-small cell lung cancer with MET exon 14 (METex14) skipping alterations. In the third quarter of 2019, tepotinib was granted breakthrough therapy status by the Food and Drug Administration (FDA), USA.
If you are trying to access new drugs for Lung Cancer that are approved outside of your country of residence, we might be able to help you access it with the help of your treating doctor. You can read more about the medicines we can help you access and their price below:
Gavreto (pralsetinib)

Retevmo (selpercatinib)
Tabrecta (capmatinib)
Zepzelca (lurbinectedin)
Tepmetko (tepotinib)
Why access a treatment for Lung Cancer with everyone.org?
everyone.org is registered in The Hague with the Dutch Ministry of Health (registration number 16258 G) as a pharmaceutical wholesale distributor. We have helped patients from over 85 countries to access thousands of medicines including. With a prescription from your treating doctor, you can count on our expert team to safely and legally guide you to access a new Lung Cancer treatment. If you or someone you know are looking to access a medicine that is not yet approved where they live, we can support you. Contact us for more information.
References:
- Cdc.gov
- Verywellhealth.com
- Cdc.gov
- Gavreto (pralsetinib) - Thesocialmedwork.com
- Retevmo (selpercatinib) - Thesocialmedwork.com
- Tabrecta (capmatinib) - Thesocialmedwork.com
- Zepelca (lurbinectedin) - Thesocialmedwork.com
- Tepmetko (tepotinib) - Thesocialmedwork.com
Disclaimer: This article is not meant to influence or impact the care provided by your treating physician. Please do not make changes to your treatment without first consulting your healthcare provider. This article is not intended to diagnose or treat illness or to influence treatment options. everyone.org is as diligent as possible in compiling and updating the information on this page. However, everyone.org does not guarantee the correctness and completeness of the information provided on this page.