Nieuw goedgekeurde medicijnen voor taaislijmziekte
Laatst bijgewerkt: 16 november 2020
U kunt legaal toegang krijgen tot nieuwe geneesmiddelen, zelfs als ze niet zijn goedgekeurd in uw land.
Leer hoeCystic fibrosis is een zeldzame, levensbedreigende genetische aandoening die wereldwijd meer dan 70.000 mensen treft. Het wordt veroorzaakt door een mutatie van het CFTR-gen, dat het zout- en watertransport in het lichaam regelt. De CFTR-mutatie laat te veel zout en water toe in de cellen. Dit resulteert in een opeenhoping van dik, kleverig slijm in de buizen en doorgangen van het lichaam. Deze verstoppingen beschadigen de longen, het spijsverteringsstelsel en andere organen. De symptomen beginnen in de vroege kinderjaren en omvatten aanhoudende hoest, terugkerende borst- en longinfecties en een slechte gewichtstoename.
Er zijn tegenwoordig verschillende behandelingen die helpen bij de behandeling van Cystic Fibrosis. Het nieuwste medicijn dat door het Europees Medisch Agentschap (EMA) is goedgekeurd voor Cystic Fibrosis is Kaftrio (elexacaftor/tezacaftor/ivacaftor).
De goedkeuring van Kaftrio (elexacaftor/tezacaftor/ivacaftor) door de EMA in augustus 2020 komt na de goedkeuring van Trikafta (elexacaftor/tezacaftor/ivacaftor; ivacaftor) in oktober 2019.
Hier volgt een overzicht van elk geneesmiddel om u en uw arts te helpen bij het nemen van een beslissing over de behandeling voor Cystic Fibrosis:
Trikafta elexacaftor/tezacaftor/ivacaftor; ivacaftor)
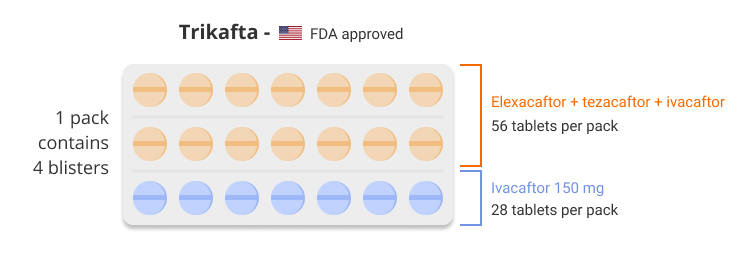
Op 21 oktober 2019 werd Trikafta elexacaftor/tezacaftor/ivacaftor; ivacaftor) goedgekeurd door de Food and Drug Administration (FDA), VS, voor de behandeling van mensen van 12 jaar en ouder met bepaalde vormen van taaislijmziekte (CF).
Trikafta (elexacaftor/tezacaftor/ivacaftor; ivacaftor) is een combinatie van ivacaftor, tezacaftor en elexacaftor en is geïndiceerd voor de behandeling van cystische fibrose (CF) bij patiënten van 12 jaar en ouder die ten minste één F508del-mutatie hebben in het gen voor cystische fibrose transmembraangeleiding (CFTR). Het is beschikbaar in combinatie tabletten met vaste dosering die elexacaftor 100 mg, tezacaftor 50 mg en ivacaftor 75 mg bevatten, en tabletten met ivacaftor 150 mg.
Kaftrio (elexacaftor/tezacaftor/ivacaftor)
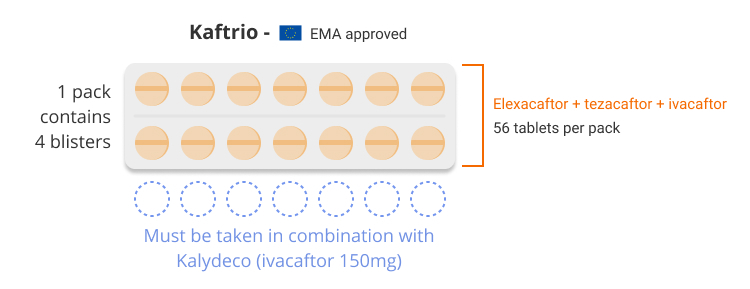
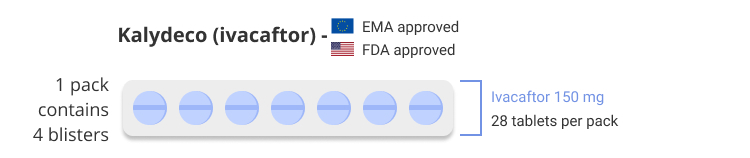
Op 21 augustus 2020 ontving Kaftrio (elexacaftor/tezacaftor/ivacaftor) een EMA-markttoelating die geldig is in de hele EU voor gebruik in combinatie met Kalydeco (ivacaftor) voor de behandeling van mensen ouder dan 12 jaar met bepaalde vormen van taaislijmziekte (CF).
Kaftrio (elexacaftor/tezacaftor/ivacaftor) is geïndiceerd in een combinatieregime met ivacaftor 150 mg tabletten (niet in de verpakking) voor de behandeling van cystische fibrose (CF) bij patiënten van 12 jaar en ouder die ten minste één F508del-mutatie hebben in het gen voor cystische fibrose transmembraangeleidingregulatie (CFTR). Het is beschikbaar als combinatiepillen met vaste dosering die elexacaftor 100 mg, tezacaftor 50 mg en ivacaftor 75 mg bevatten.
Je kunt de volledige infographic over geneesmiddelen hier downloaden.
Als u of iemand die u kent toegang wil krijgen tot Trikafta elexacaftor/tezacaftor/ivacaftor; ivacaftor) of Kaftrio (elexacaftor/tezacaftor/ivacaftor) in combinatie met Kalydeco, kunnen wij u helpen.
Neem contact op met ons Patiënt Support Team voor meer informatie.