Wanneer is Vamorolone verkrijgbaar in Europa en het Verenigd Koninkrijk? Het volledige verhaal.
Laatst bijgewerkt: 16 april 2024

U kunt legaal toegang krijgen tot nieuwe geneesmiddelen, zelfs als ze niet zijn goedgekeurd in uw land.
Leer hoeCorticosteroïden zijn al vele jaren een standaardbehandeling voor patiënten met Duchenne spierdystrofie. Meestal worden ze in het behandelplan opgenomen rond de leeftijd van 4 of 5 jaar, voordat ze de "plateaufase" ingaan en een aanzienlijk krachtverlies ervaren 1. Helaas kan langdurig gebruik van corticosteroïden geassocieerd worden met verschillende bijwerkingen, waaronder gedragsproblemen, gewichtstoename, osteoporose en meer 2.
In deze context is de recente goedkeuring door de FDA van Agamree (vamorolone) als een "corticosteroïde van de nieuwe generatie" met minder bijwerkingen een broodnodige doorbraak in de behandeling van Duchenne.
Hoewel vamorolone al in het eerste kwartaal van 2024 in de Amerikaanse apotheken wordt verwacht, is het nog nergens anders goedgekeurd.
Wanneer is vamorolone verkrijgbaar in Europa en het Verenigd Koninkrijk? Hier is alles wat je moet weten.
Waar wordt vamorolon voor gebruikt?
Agamree (vamorolon) is geïndiceerd voor de behandeling van kinderen (4+) en volwassenen met Duchenne spierdystrofie.
Agamree is een dissociatief corticosteroïde. Het werkt voornamelijk door ontstekingen in het lichaam te kalmeren. Vamorolone werkt op dezelfde manier als andere corticosteroïden. Het hecht zich echter anders aan cellen en activeert bepaalde reacties van het lichaam niet zoals andere steroïden doen.
Het is niet helemaal duidelijk hoe vamolorone werkt bij DMD (Duchenne spierdystrofie). Klinische onderzoeksresultaten suggereren echter dat het kinderen met deze aandoening helpt om sneller op te staan en beter te lopen. Enkele gebruikelijke bijwerkingen zijn er opgezwollen uitzien, overgeven, aankomen en zich chagrijnig voelen 3.
Is vamorolone goedgekeurd door de EMA?
Sinds december 2023 is Agamree (vamorolon) goedgekeurd door het EMA voor de behandeling van Duchenne spierdystrofie bij volwassenen en kinderen ouder dan 4 jaar 3.
Wanneer zal vamorolone verkrijgbaar zijn in Europa?
Hoewel de goedkeuring van vamorolone door de EMA goed nieuws is, betekent dit niet dat het medicijn meteen in alle Europese landen beschikbaar zal zijn. Voordat het de apotheken bereikt, moeten de fabrikant van het medicijn en de lokale gezondheidsautoriteit van elke lidstaat beslissingen nemen over lokale goedkeuring, prijzen en dekking door de ziektekostenverzekering. Als gevolg hiervan zal vamorolone waarschijnlijk op verschillende momenten beschikbaar zijn in elk land binnen Europa.
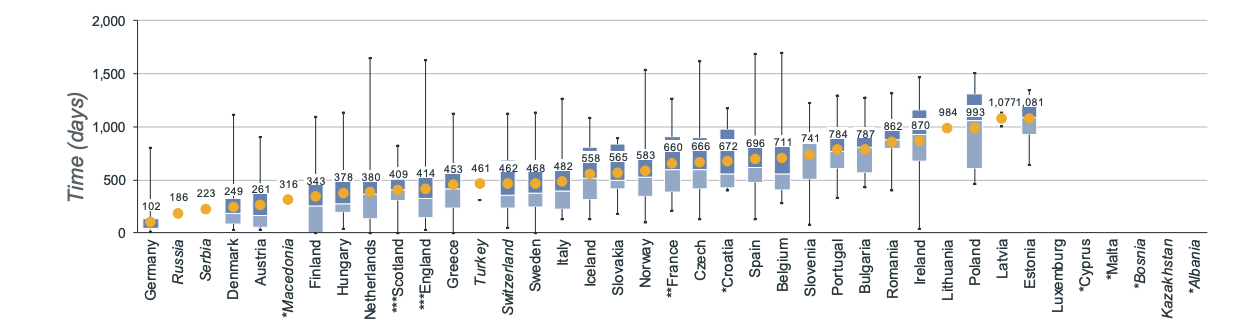
Na goedkeuring door de EMA duurt het gemiddeld 511 dagen voordat nieuwe geneesmiddelen in de hele EU beschikbaar zijn. Deze tijdlijn verschilt enorm per land. Voor weesgeneesmiddelen zoals vamorolone varieert dit van 102 dagen in Duitsland tot 1.081 dagen in Estland 5.
Wanneer is vamorolone verkrijgbaar in het Verenigd Koninkrijk?
Na de goedkeuring door de EMA is vamoroline nu ook goedgekeurd door de MHRA in het VK. Dit maakt het geneesmiddel de eerste Duchenne behandeling die is goedgekeurd in het Verenigd Koninkrijk, de EU en de VS samen.
Voordat vamorolone beschikbaar is op de NHS, moet NICE zijn beslissing over dit onderwerp herzien en publiceren. Er zijn raadplegingen gaande en een ontwerprichtlijn wordt eind april 2024 verwacht6 . Indien positief, zou Agamree binnen 3 maanden na de beslissingsdatum van NICE beschikbaar moeten zijn voor patiënten.
Goedkeuringsstatus van Vamorolone in de rest van de wereld
Vanaf april 2024 is Agamree (vamorolon) nergens anders ter wereld goedgekeurd voor de behandeling van Duchenne spierdystrofie 7.

Manieren om veilig toegang te krijgen tot Agamree (vamorolone) voordat het is goedgekeurd in uw land
Ben je een Duchenne patiënt buiten de VS? Als uw arts denkt dat vamorolon u zou kunnen helpen, hoeft u misschien niet te wachten op de lokale goedkeuring of beschikbaarheid van Agamree. In plaats daarvan kunnen uw arts en u klinische proeven met vamorolone onderzoeken. Je kunt vamorolone ook meteen kopen als individuele patiënt op naam.
Doe mee aan een klinisch onderzoek met vamorolone
U kunt deelnemen aan een klinisch onderzoek om Agamree (vamorolon) of andere niet-goedgekeurde geneesmiddelen te krijgen. Het vinden van een onderzoek dat deelnemers werft in uw land kan moeilijk zijn, maar het is mogelijk. Om deel te nemen aan het onderzoek, moet u voldoen aan de toelatingscriteria. U hebt ook de steun van uw behandelend arts nodig.
Hier zijn enkele goede plaatsen om te beginnen met zoeken naar lopende klinische onderzoeken naar vamorolon:
- ClinicalTrials.gov: Dit is een database met alle klinische onderzoeken in de VS. Sommige onderzoeken staan ook open voor internationale deelnemers. Een voorbeeld is het klinische onderzoek NCT5185622 met vamorolone, waarvoor patiënten in Canada worden geworven 8.
- EUClinicaltrials.eu: Deze database bevat alle klinische onderzoeken in de Europese Unie. Momenteel bevat deze beperkte informatie over onderzoeken die vóór 31 januari 2022 zijn gestart. Voor deze onderzoeken kunt u het EU Clinical Trials Register raadplegen.
- myTomorrows: Deze organisatie ondersteunt patiënten bij het vinden van behandelingsmogelijkheden in klinische onderzoeken.
Koop vamorolone op individuele basis van patiënt op naam
In de meeste landen mogen patiënten legaal geneesmiddelen kopen en importeren die hun leven kunnen verbeteren of levensbedreigende aandoeningen aanpakken. Als u toegang wilt krijgen tot vamorolone voordat het in uw land beschikbaar is, kan dit een optie zijn voor u en uw arts.
De verordening die dit mogelijk maakt staat bekend als de verordening betreffende de invoer van individuele patiënten op naam. De specifieke administratieve vereisten kunnen per land verschillen. In alle gevallen moet echter aan deze criteria worden voldaan:
-
Het geneesmiddel in kwestie is goedgekeurd voor de markt in een ander land en is (nog) niet goedgekeurd of beschikbaar in het land van de patiënt;
-
Er is geen alternatief op de lokale markt;
-
Het medicijn is voor persoonlijk gebruik;
-
De patiënt heeft een voorschriftbrief van zijn behandelend arts;
-
De arts neemt de verantwoordelijkheid voor de behandeling. Dit kan van land tot land verschillende documentatie vereisen.
Wil je gebruik maken van de invoerregeling voor individuele patiënten om vamorolone te krijgen voordat het algemeen verkrijgbaar is in Europa, het VK of elders? Dan moet je eerst je behandelend arts raadplegen en een geschikt recept krijgen.
Heb je al een recept? Ons team kan je direct helpen bij het kopen van vamorolone.
Referenties:
- Steroïden (corticosteroïden). Ouderproject Spierdystrofie, geraadpleegd op 13 november 2023.
- Side Effects of Long Term High-Dose Steroid Therapy, geraadpleegd op 13 november 2023.
- Agamree: Goedgekeurd door het Europees Geneesmiddelenbureau. Europees Geneesmiddelenbureau, 13 oktober 2023.
- EU-handelsvergunning aanvragen voor geneesmiddelen voor menselijk gebruik. Europees Geneesmiddelenbureau, geraadpleegd op 13 november 2023.
- EFPIA Patiënten W.A.I.T. Indicator 2021 Enquête. Efpia, geraadpleegd op 13 november 2023.
- Projectinformatie | Vamorolon voor de behandeling van Duchenne spierdystrofie [ID4024] | Richtlijn. NICE, geraadpleegd op 13 november 2023.
- AGAMREE® (vamorolon) - santhera. Santhera, geraadpleegd op 13 november 2023.
- A Study to Assess Vamorolone in Boys Ages 2 to <4 Years and 7 to <18 Years With Duchenne Muscular Dystrophy (DMD). ClinicalTrials.gov, Accessed 13 November 2023.