Kan Enhertu darmkanker behandelen? Laatste resultaten, tijdlijnen voor goedkeuring en meer.
Laatst bijgewerkt: 15 juli 2024
U kunt legaal toegang krijgen tot nieuwe geneesmiddelen, zelfs als ze niet zijn goedgekeurd in uw land.
Leer hoeSinds de eerste goedkeuring door de FDA in 2019, Enhertu heeft het veel aandacht gekregen in de oncologische wereld. In 2023 zet Enhertu zijn indrukwekkende traject voort met nog eens twee doorbraakaanwijzingen van de FDA. Het heeft nu een totaal van zeven 1.
Een van de laatste successen van Enhertu is de goedkeuring als kankerdiagnostische behandeling. Dit betekent dat het nu kan worden toegepast op alle patiënten met HER2-dragende tumoren, inclusief colorectale tumoren. Voor alle patiënten met dikkedarmkanker is dit een belangrijke mijlpaal. Tegelijkertijd roept het veel vragen op.
Dit is alles wat je moet weten over Enhertu voor darmkanker.
Is Enhertu door de FDA goedgekeurd voor darmkanker?
Ja. In april 2024 werd Enhertu goedgekeurd voor gebruik bij alle kankertypes met HER2-expressie. Dit omvat ook colorectale kanker.
Voor welke soorten kanker is Enhertu goedgekeurd?
Enhertu is momenteel goedgekeurd door de EMA in Europa voor de behandeling van:
- HER2-positieve uitgezaaide borstkanker die niet operatief verwijderd kan worden;
- HER2-arme uitgezaaide borstkanker die niet met een operatie kan worden verwijderd;
- HER2-positieve gevorderde maagkanker of kanker van de gastro-oesofageale junctie 4.
In de VS is Enhertu bovendien goedgekeurd voor de behandeling van:
- HER2-mutante uitgezaaide niet-kleincellige longkanker 5.
- alle HER2-drukkende vaste tumoren.
Hoe effectief is Enhertu voor darmkanker?
Omdat Enhertu een gerichte therapie is, is deze alleen van toepassing op kankers met een HER-2 expressie. Ongeveer 3-5% van alle colorectale kankers vallen in deze categorie 6.
Resultaten klinisch onderzoek
In juni 2023 werden de definitieve resultaten van de DESTINY-CRC01 studie gepubliceerd. Deze fase 2-studie richtte zich op het beoordelen van de werkzaamheid en veiligheid van Enhertu bij patiënten met HER2-expressie van uitgezaaide dikkedarmkanker. De patiënten in de studie hadden tumoren die progressie vertoonden na ten minste 2 eerdere behandelingsrondes 7.
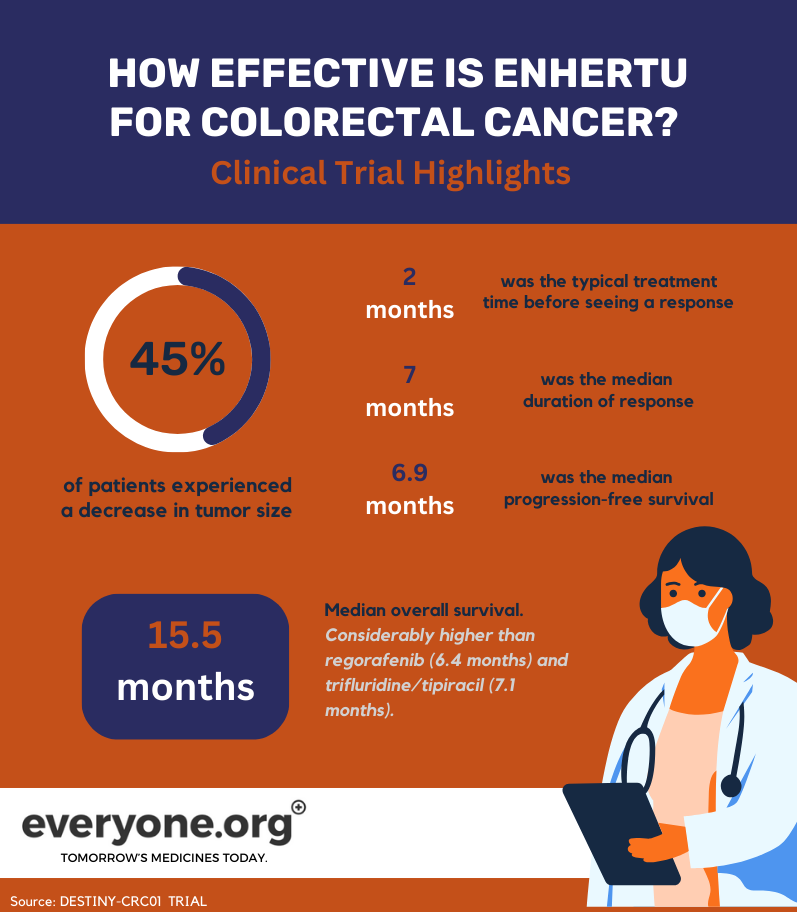
De belangrijkste uitkomsten van dit onderzoek voor patiënten met dikkedarmkanker waren:
-
Bij 45,3% van de patiënten die behandeld werden met Enhertu kromp de tumor gedeeltelijk;
-
De respons op de behandeling was meestal ongeveer 2 maanden na aanvang van de behandeling zichtbaar;
-
De mediane duur van de respons was 7 maanden;
-
De mediane progressievrije overleving was 6,9 maanden;
-
De mediane totale overleving was 15,5 maanden. Dit resultaat ligt aanzienlijk hoger dan de huidige zorgstandaard. regorafenib en trifluridine/tipiracil zijn bijvoorbeeld veelgebruikte therapieën in de derde lijn. Deze behandelingen hebben een totale overleving van respectievelijk 6,4 maanden en 7,1 maanden 7.
Een andere studie, genaamd DESTINY-CTC02, bestudeert Enhertu voor patiënten met dikkedarmkanker. De studie is nog gaande, maar de voorlopige resultaten zijn in lijn met de uitkomsten van de DESTINY-CTC01 studie 10.

Hoe veilig is Enhertu voor darmkanker?
Op het gebied van veiligheid zijn dit de belangrijkste resultaten van de DESTINY-CRC01 studie:
-
Elke patiënt had een bijwerking van de behandeling. De meest voorkomende bijwerkingen waren maag- en bloedproblemen.
-
Ernstige bijwerkingen traden op bij 37,7% van de patiënten. De meest voorkomende ernstige bijwerkingen waren een laag aantal neutrofielen (22,1%) en anemie (14%) 7.
-
Een bijwerking genaamd interstitiële longziekte (ILD) werd geassocieerd met het stoppen van het geneesmiddel en werd waargenomen bij 7% van de patiënten.
-
Er werden 3 geneesmiddelgerelateerde sterfgevallen gemeld, die allemaal in verband werden gebracht met interstitiële longziekte.
Wat betekent dit?
EnhertuDe veiligheidsresultaten kunnen niet direct worden vergeleken tussen verschillende patiëntengroepen. Maar om u te helpen een en ander in de juiste context te plaatsen, volgt hier een samenvatting van de veiligheidsresultaten van Enhertu voor meerdere tumortypen. Inclusief tumoren waarvoor Enhertu is goedgekeurd:
-
ILD trad op bij 12% van de proefpatiënten, met fatale afloop in 1,5% van de gevallen;
-
Verlaagde neutrofiele aantallen kwamen voor bij 34,6% van de proefpatiënten;
-
Bloedarmoede kwam voor bij 34-43% van de proefpatiënten (afhankelijk van de medicatiedosering) 8.
Gezien dit feit is het veiligheidsprofiel van Enhertu voor colorectale kanker vergelijkbaar met het profiel voor andere goedgekeurde kankers.
Wanneer wordt Enhertu goedgekeurd voor darmkanker?
Enhertu is al goedgekeurd door de FDA voor HER2-positieve colorectale kanker - een indicatie die valt binnen de laatste FDA-goedkeuring van Enhertu.
Deze laatste goedkeuring is echter alleen een feit in de VS. Wat betekent dit voor darmkankerpatiënten elders? Welke rol zou Enhertu kunnen spelen in jouw CRC-behandeling?
Kan mijn arts Enhertu voorschrijven voor darmkanker?
Het korte antwoord is ja.
Enhertu is al goedgekeurd door de FDA voor de behandeling van HER2-positieve dikkedarmkanker. Zelfs als je in een ander land woont, heeft je arts de bevoegdheid om het medicijn toch voor deze indicatie voor te schrijven. Hij of zij zou dit kunnen doen op basis van de eindresultaten van de DESTINY-CRC01 trial of de voorlopige resultaten van de DESTINY-CRC02 trial, en op basis van de specifieke kenmerken van jouw geval.
Als een arts je een medicijn geeft voor een ziekte waarvoor het niet lokaal is goedgekeurd, dan is dat off-label gebruik. In sommige landen kan het lastig zijn om een recept voor off-label gebruik te krijgen vanwege lokale regelgeving en beschikbaarheid. Het is echter altijd mogelijk om het te vullen met behulp van de Named Patient Import-regeling.
Heeft uw arts besloten om Enhertu voor te schrijven voor de behandeling van uw darmkanker? Ons team op www.everyone.org kan u helpen toegang te krijgen tot het medicijn. Wij zijn gespecialiseerd in het vinden en leveren van voorgeschreven medicijnen die niet zijn goedgekeurd of niet beschikbaar zijn in het land van de patiënt. Neem contact met ons op, zodat we u kunnen helpen.
Referenties:
- Barrie, Robert. Enhertu wint twee doorbraaktherapie-aanduidingen van de FDA. Farmaceutische Technologie, 31 augustus 2023.
- FDA kent doorbraaktherapieaanwijzingen toe aan Trastuzumab Deruxtecan voor HER2+ solide tumoren, inclusief mCRC. OncLive, 31 augustus 2023.
- Doorbraaktherapie. FDA, 4 januari 2018.
- Enhertu |Europees Geneesmiddelenbureau. Europees Geneesmiddelenbureau, geraadpleegd op 30 oktober 2023.
- Stewart, Judith. Enhertu (fam-trastuzumab deruxtecan-nxki) FDA Goedkeuringsgeschiedenis. Drugs.com, 15 augustus 2022.
- HER2 Biomarker bij darmkanker. Ken uw biomarker, 24 mei 2023.
- Definitieve resultaten van DESTINY-CRC01, een onderzoek naar trastuzumab deruxtecan bij patiënten met HER2-expressie van uitgezaaide dikkedarmkanker. Nature Communications, geraadpleegd op 30 oktober 2023.
- Enhertu, INN-trastuzumab deruxtecan. Europees Geneesmiddelenbureau , geraadpleegd op 30 oktober 2023.
- Trastuzumab Deruxtecan bij deelnemers met HER2-overexpressie van gevorderde of gemetastaseerde colorectale kanker (DESTINY-CRC02). ClinicalTrials.gov, geraadpleegd op 30 oktober 2023.
- Trastuzumab deruxtecan (T-DXd) bij patiënten (pts) met HER2-overexpressie/amplificatie (HER2+) van metastatisch colorectaalcarcinoom (mCRC): Primaire resultaten van de multicenter, gerandomiseerde, fase 2-studie DESTINY-CRC02. Tijdschrift voor Klinische Oncologie, geraadpleegd op 30 oktober 2023.